Коллектив исследователей Института биофизики будущего МФТИ впервые в мире напрямую измерил и количественно оценил процесс формирования самых первых, зачаточных электрических контактов между пересаженными кардиомиоцитами и тканью сердца-реципиента. Это фундаментальное открытие, опубликованное в журнале Polymers, проливает свет на критически важный и ранее не изученный этап клеточной терапии сердца, напрямую влияющий на ее эффективность и безопасность.
Исследование выполнено при поддержке междисциплинарного гранта РНФ в коллаборации с НМИЦ им. ак. Е. Н. Мешалкина и НМИЦ ТИО им. ак. В. И. Шумакова.
Сердечно-сосудистые заболевания остаются одной из основных причин смертности в мире. Дегенерация миокарда до сих представляет собой серьезную проблему для медицины, а терапевтические стратегии на основе клеток открывают многообещающие возможности для лечения сердечных патологий. Одним из перспективных направлений является трансплантация кардиомиоцитов — клеток сердечной мышцы — для восстановления поврежденных участков миокарда после инфаркта. Однако их клиническое применение по-прежнему ограничено недостаточной эффективностью приживления, высокими потерями при доставке клеток и осложнениями, возникающими из-за нарушения электромеханической интеграции.
Проблема состоит и в том, что даже если пересаженные клетки приживаются, они далеко не всегда синхронизируют свою работу с окружающей тканью. Нескоординированные сокращения новых клеток могут стать источником опасных аритмий, сводя к нулю терапевтический эффект. Таким образом, хороший результат требует не только выживания клеток и их интеграции, но и установления функциональной электромеханической связи с тканью реципиента.
Для решения этой проблемы необходимо знать, каким образом в первые минуты после трансплантации между новыми клетками и «хозяевами» начинают устанавливаться электрические мосты. До сих пор у науки не было инструментов, чтобы зафиксировать и измерить этот процесс в реальном времени.
Группа исследователей под руководством Константина Агладзе и Валерии Цвелой ответила на этот вопрос, создав функциональную и минималистичную экспериментальную модель. Они взяли за основу подход, сосредоточенный на самых истоках клеточной коммуникации.
«Наше исследование посвящено тому, как клетки сердца образуют между собой контакты. Это весьма острый вопрос для ученых, поскольку сейчас актуальны исследования в области тканевой инженерии сердца, например терапия инфарктов или разработка биологических кардиостимуляторов, которые требуют четкого понимания процесса взаимодействия новых клеток кардиостимуляторов с собственными кардиомиоцитами пациентов. Для ответа на этот вопрос мы разработали модель, которая позволяет исследовать то, как образуются контакты на крысиных клетках сердца»,— рассказал о работе Виталий Джабраилов, инженер лаборатории экспериментальной и клеточной медицины МФТИ.
В ходе исследования ученые вырастили сплошной слой кардиомиоцитов, имитирующий здоровую ткань сердца-реципиента. Затем они поместили на этот «газон» отдельные клетки, предварительно «усадив» их на микроскопические волокна из биосовместимого полимера — поликапролактона (PCL). Эти волокна, натянутые на рамку из инертного силикона PDMS, играли роль стабилизирующих лесов, не позволяющих клетке свободно плавать и дающих ей возможность подготовиться к установлению контактов. Это ключевое условие, ведь клетка в суспензии не может вступить в полноценное электромеханическое взаимодействие.
«Мы хотели воспроизвести в чистом виде самый ранний этап интеграции, когда пересаженная клетка только-только касается ткани-хозяина. Наши волокна — не имитация сложного внеклеточного матрикса, а скорее простая механическая опора, катализирующая внутреннюю способность клетки к самоорганизации. Это как надежная страховочная веревка для альпиниста»,— поясняет Валерия Цвелая, заведующая лабораторией экспериментальной и клеточной медицины МФТИ.
Чтобы увидеть, как рождается электрическая связь, ученые применили метод оптического картирования. Клетки обработали флуоресцентным красителем, чувствительным к ионам кальция, концентрация которых резко возрастает при прохождении электрического импульса. Таким образом, распространение волны возбуждения по монослою и ее переход на новую клетку можно было наблюдать в виде вспышек свечения под микроскопом в режиме реального времени. Огромный массив данных обрабатывался с помощью нейронной сети SUPPORT, которая эффективно отсеивала шумы и повышала четкость сигнала, что было критически важно для точных измерений.
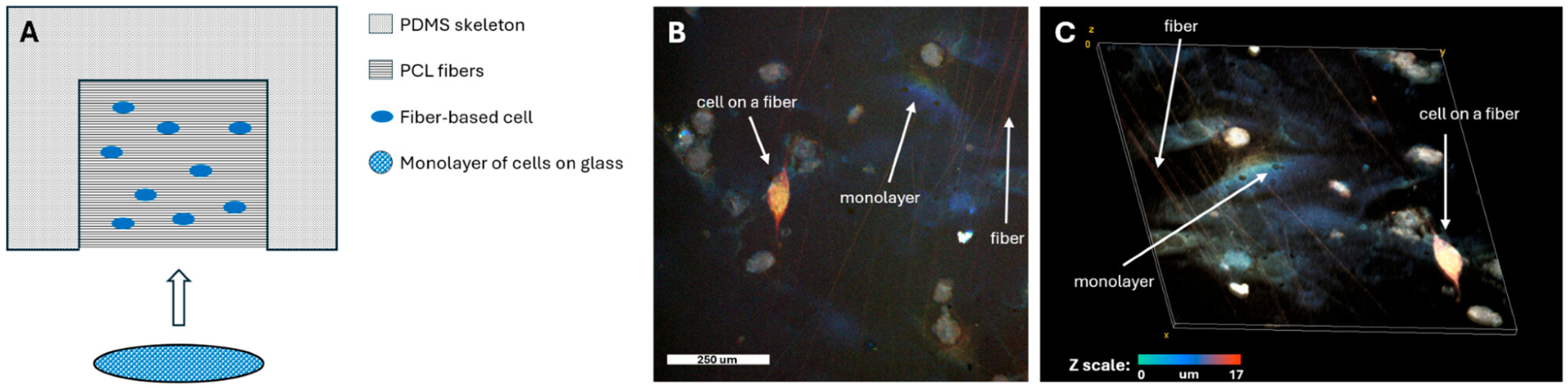
Рисунок. Схема эксперимента и посев волоконно-культивируемых клеток на синхронизированный монослой: (A) схема разработанной модели для изучения формирования электрофизиологических контактов между клетками; (B) двумерное конфокальное изображение клеточного монослоя с посеянными сверху волокнами; (C) трехмерное конфокальное изображение клеточного монослоя с посеянными сверху волокнами. На панелях (B, C) используется общая цветовая шкала высоты (z-шкала). Источник: Polymers
«В ходе исследования нам впервые удалось измерить функциональный дефицит интеграции в его „чистом” виде, в первые минуты и часы. Мы получили конкретный числовой тест производительности: в течение первых трех часов начальные соединения в 39–44 раза менее эффективны в передаче возбуждения, чем зрелые контакты в естественном монослое. Это объясняет, почему в экспериментах клетки на волокнах синхронизировали свои сокращения с подложкой лишь в 46% случаев, то есть реагировали примерно на каждый второй импульс.
Таким образом, наша работа представляет собой первое прямое измерение функционального дефицита в первые минуты и часы интеграции трансплантата. Это принципиально новая информация для моделирования рисков аритмий при клеточной терапии. Теперь мы знаем, что есть окно в несколько часов, когда пересаженная ткань электрически уязвима, и эту уязвимость можно и нужно учитывать»,— подчеркнула Валерия Цвелая.
Результаты исследования дали точный количественный ответ на главный вопрос: как в первые часы зарождающиеся межклеточные связи проводят электрический импульс? Более того, была измерена задержка в передаче сигнала: волне возбуждения требовалось в среднем на 290 мс больше, чтобы «перепрыгнуть» на клетку-трансплантат.
«Хотя на данный момент наше исследование носит скорее фундаментальный характер, но мы уже на практике знаем, что примерно в течение трех часов клетки, расположенные на специальных носителях, подготовлены к образованию первичных контактов с сердечной тканью, и на них передается ее возбуждение. Полученные данные — основа для создания более безопасных протоколов клеточной терапии сердца и в перспективе открывает путь к созданию новых гибридных тканеинженерных конструктов»,— заключил Виталий Джабраилов.
Новизна исследования заключалась и в самом подходе. Ученые показали, что для запуска сложнейшего биологического процесса — установления электрического диалога между клетками — может быть достаточно простой синтетической полимерной подложки, а не воссоздания всей сложности природного клеточного окружения. Простые инертные полимерные волокна могут выступать в качестве каталитической основы для этого фундаментального биологического процесса, предлагая эффективную стратегию для контроля интеграции искусственных тканей.
Кроме того, ученые продемонстрировали прототип еще более мощного метода — трехмерного оптического картирования на конфокальном микроскопе, который в будущем позволит с очень высокой детализацией наблюдать за распространением волн возбуждения в объемных тканевых конструктах.
Научная статья: Vitalii Dzhabrailov, Elena Turchaninova, Daria V. Kononova, Egor Ilin, Mikhail Slotvitsky, Anton Efimov, Igor Agapov, Valeriya Tsvelaya, Alexander Romanov, Konstantin Agladze; Quantifying Early Electrochemical Integration of Cardiomyocytes Using a Minimalist PCL Nanofiber Platform; Polymers, 2025. DOI: 10.3390/polym18010017
