Саркомы — это редкие и агрессивные опухоли, которые развиваются из соединительных тканей вроде мышц и костей. Биофизики из МФТИ впервые в России создали модель роста сарком на куриных эмбрионах, а также метод высокочувствительной визуализации клеток сарком, содержащих флуоресцентные и люминесцентные метки. Это поможет не только описать рост опухоли, но и проверить, как его можно замедлить и даже повернуть вспять. Исследование проведено при поддержке гранта РНФ (№ 23-14-00220), а его результаты опубликованы в журнале Scientific Reports.
Злокачественные новообразования встречаются все чаще по мере старения населения Земли. К счастью, многие из них поддаются лечению, в том числе благодаря терапии нового поколения. Тем не менее раковые клетки способны быстро приспосабливаться к лекарствам, что наряду с их разнообразием требует создания все новых подходов к лечению.
В своем исследовании ученые из Института биофизики будущего МФТИ и Физтех-школы биологической и медицинской физики МФТИ сосредоточились на саркомах. Это разнородная группа опухолей, которые развиваются в соединительных тканях: около 80% отмечают в мягких тканях, остальные 20% — в костях. Саркомы относят к опасным заболеваниям: скажем, пациент с остеосаркомой (саркома костной ткани) имеет лишь 50% шанса прожить еще пять лет.
Традиционно онкологические исследования проводили на лабораторных животных. Хотя такие модели помогают многое узнать о свойствах опухолей (в том числе сарком), они требуют сложных операций. К недостаткам животных моделей также относят длительность экспериментов (от 3–6 месяцев) и высокую цену каждого из них, что существенно ограничивают изучение опухоли в динамике.
Более того, в этих моделях трудно контролировать и учитывать влияние «места обитания», так называемое микроокружение опухоли. Оно включает кровеносные сосуды, находящиеся рядом ткани и клетки и выделяемые самой опухолью соединения, которые имеют ключевое значение для роста новообразования. Поэтому исследования в области онкологии требуют новые реалистичные модельные системы, которые полно воспроизводят подобные взаимодействия опухоли с «местом обитания».
Ярким примером такой модельной системы служит хорион-аллантоисная мембрана куриного эмбриона (chick embryo chorioallantoic membrane, сокращенно CAM). Это временный эмбриональный орган, образующийся у птиц, рептилий и млекопитающих при слиянии зародышевых оболочек: хориона (серозы) и аллантоиса. CAM легко изучать визуально, она имеет плотную сеть сосудов, на определенном периоде развития эмбриона не подвержена влиянию иммунной системы и отлично подходит для сравнительно быстрого (не более 2–3 недель), эффективного и доступного изучения связей опухолевых клеток с их микроокружением.
Работа ученых Физтеха опиралась на более ранние, проведенные в Гентском университете (Бельгия) эксперименты и стала их развитием. Если до того была показана эффективность CAM для исследования некоторых клеточных линий, то теперь стало возможным не только получение опухолей и метастазов из клеток практически любой линии, но и их автоматизированная визуализация. А главное — количественная оценка развития и метастазирования опухоли в масштабах целого куриного эмбриона с помощью меченых клеток.
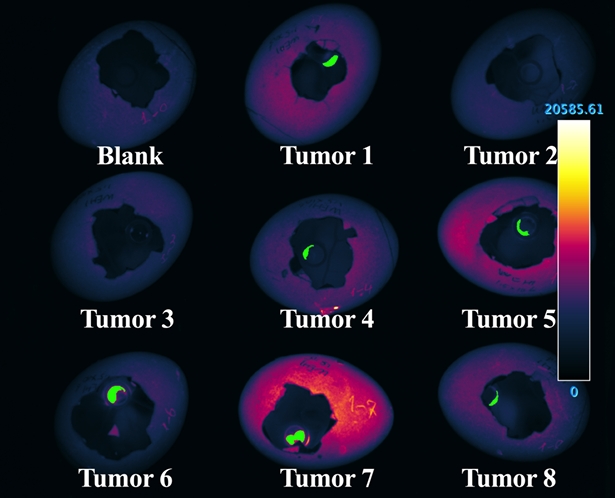
В процессе разработки модели была создана эффективная система лентивирусной доставки генетического материала, с помощью которой клеткам остеосаркомы человека и фибросаркомы мыши водили сразу две метки. Это светящийся красным цветом флуоресцирующий белок «Катюшка» (Katushka2s) и фермент NanoLuc™, полученный из глубоководной креветки и модифицированный для оптимальной работы в качестве люминесцентного репортера. При этом люминесцентные метки оказались более эффективными для выявления самых мелких новообразований.
Важно, что для ускорения роста саркомы и увеличения размеров опухоли ученые использовали специальную среду, обогащенную опухолевыми клетками. Она содержала целый набор биомолекул, выделяемых этими же опухолями вовне,— так называемый секретом. Использование такой среды для обработки CAM опробовано впервые. Введение этой среды, а также нанесение царапин на CAM перед введением опухолевых клеток позволили получить более правильные округлые опухоли. Также она ускорила формирование метастазов почти всеми испытанными клеточными линиями сарком человека и животных. В ходе исследования выяснилось, что ключевыми компонентами обогащенной среды оказались различные молекулы с регуляторной функцией — цитокины, хемокины, факторы роста и т. д.
«Особое внимание в нашем исследовании привлек фактор роста эндотелия сосудов VEGFA (Vascular endothelial growth factor A). Этот белок стимулирует образование новых сосудов в опухоли, влияет на иммунный ответ и тем самым способствует росту злокачественного новообразования. Комплексное изучение белков в составе обогащенной среды показало значительное повышение концентрации именно этого фактора роста»,— пояснил Денис Кузьмин, руководитель гранта, директор Физтех-школы биологической и медицинской физики МФТИ.
Стимулирующее действие VEGFA как «помощника опухоли» известно давно. В клинике его влияние обычно нейтрализуют с помощью препарата Авастин (Avastin). Это антитела, избирательно связывающие VEGFA, которые существенно замедляют рост опухоли за счет блокировки роста сосудов, снабжающих ткань опухоли. В новой работе ученые использовали Авастин, чтобы проверить значимость этого фактора для разрастания опухоли на поверхности САМ. Препарат существенно снизил стимулирующий эффект обогащенной среды на рост опухоли, что видно по снижению прорастания в нее сосудов и значительно меньшему числу метастазов.
Таким образом, исследование указало на большое значение секретома опухоли для увеличения ее кровеносной сети и формирования «среды обитания», способствующей ее росту. При этом фактор VEGFA представляет собой перспективную мишень для вмешательства в процесс прорастания сосудов опухоли.
«Важно подчеркнуть, что использование Авастина в широкой клинической практике имеет много ограничений. Выявленные нами в составе обогащенной среды другие факторы роста также являются потенциальными мишенями для терапии, направленной против разрастания кровеносных сосудов (ангиогенеза) опухоли.
Разработанная нами модель позволила продолжить изучение этих перспективных факторов-мишеней, а также уже доказала свою применимость не только для исследования сарком, но и для немелкоклеточного рака легких и рака молочной железы человека. Таким образом, наша модель дает онкологам уникальный инструмент для достаточно быстрой оценки эффективности как новых препаратов против опухолевого ангиогенеза, так и против местазирования клеток других видов рака»,— прокомментировал ответственный исполнитель работ Сергей Леонов, заместитель руководителя лаборатории персонализированной химио-радиотерапии Института биофизики будущего МФТИ.
В работе кроме сотрудников лаборатории персонализированной химио-радиотерапии Института биофизики будущего МФТИ и Физтех-школы биологической и медицинской физики МФТИ принимали участие их коллеги из ФИЦ Оригинальных и перспективных биомедицинских и фармакологических технологий и Института биофизики клетки РАН (Пущино).
